邮箱地址
前沿资讯
发布时间:2023-10-30 09:46:33 作者:青岛海大海洋寡糖科技有限公司 来源:本站
文章题目:Enzymatic synthesis of low molecular weight heparins from N-sulfo heparosan depolymerized by heparanase or heparin lyase
发表期刊 :Carbohydrate Polymers
影响因子 : 10.723(2021)
通讯单位 : 伦斯勒理工学院 浙江工业大学药学院

普通肝素 (UFH) 和低分子量肝素 (LMWH) 均来源于猪肠黏膜,已经作为抗凝剂在临床上被广泛使用。LMWH 是通过UFH的受控化学或酶促降解来获得的,与UFH 相比,LMWH显示出更高的生物利用度、更长的半衰期、可预测的药代动力学和降低诱发血小板减少症的优势,并应用于治疗静脉血栓栓塞和其他凝血异常。
由于肝素来源依赖于脆弱的动物种群(生猪),猪瘟的流行会严重危害肝素的稳定供应,因此迫切需要开发新的肝素替代来源。在这篇文章中,作者报道一种LMWH的化学生物催化合成方法。该方法以E. coli K5来源的heparosan为原料,使用HepBp或HepIII 酶促降解以获得合适分子量的底物,最后通过差向异构酶和磺基转移酶处理后获得还原端饱和或不饱和的LMWH。
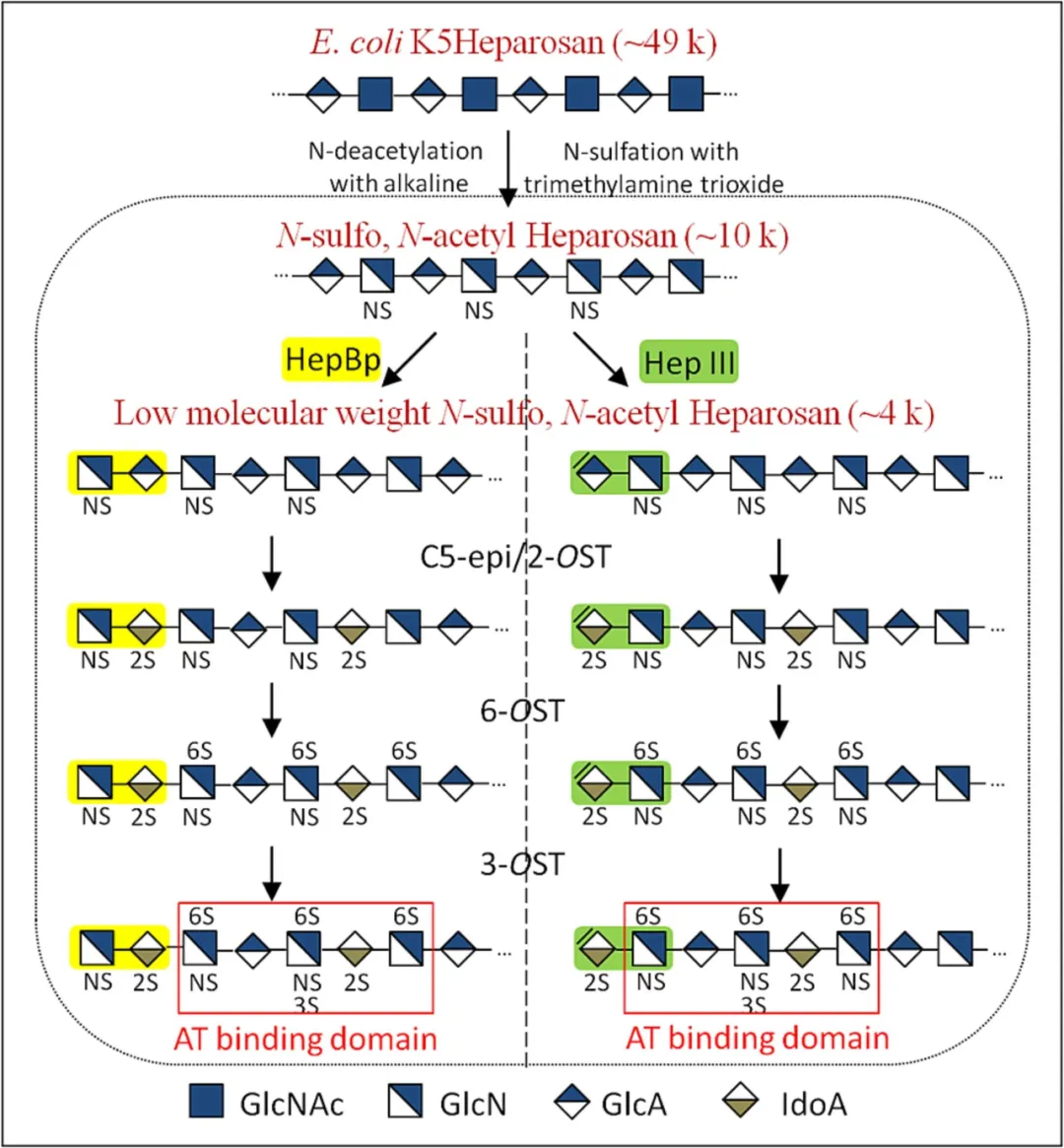
图1:使用HepBp和HepIII降解酶促生物合成LMWH
作者首先使用HepBp或HepIII来降解heparosan获得目标分子量为 3.8 至 4.5 kDa 的 LMW-NSH(Low molecular weight ,N-sulfo,N-acetyl heparosan),并对底物量、酶量和反应时间进行了优化。其中,HepBp的最佳酶消化条件是:100 μg NSH底物在100 μL 50 mM乙酸铵缓冲液 (pH = 4.5) 中用2 μL HepBp (0.7 mg/mL)在37°C下处理15分钟,最终获得的LMW-NSH的Mw为3950±30 Da(图 2E);HepIII的最佳酶消化条件是:100 μg NSH底物在50 mM乙酸铵缓冲液 (pH = 7.0) 中用5 μL HepIII (10 U/mg) 在37°C下处理5分钟。获得的LMW-NSH的Mw为4250 ± 50 Da(图 2F)。

图2:通过 GPC 分析的LMWH分子量分布。A.依诺肝素分子量校准物;B.依诺肝素;C和D.NSH原料;E.HepBp裂解LMW-NSH;F.HepIII裂解LMW-MSH;G.LMWH(HepBp);H.LMWH(HepIII)。
接下来作者通过酶促反应步骤,实现LMW-NHS向LMWH的转化。首先,使用差向异构酶和磺基转移酶2-OST以提供 IdoA2S。其中,以HepBp降解获得LMW-NSH为底物,2-OST的催化效率高于80%;以HepIII降解获得LMW-NSH 为底物,2-OST的催化效率为68%,这可能是由于非还原端不饱和糖醛酸的存在会抑制2-OST的催化活性(图 3A)。接下来,以LMW-NS2SH为底物,继续使用6-OST和3-OST处理,并以高收率获得两种LMWH(图 3B和3C)。抗凝活性分析和分子量测定分析发现,两种LMWH均表现出与依诺肝素相似的抗Xa因子和抗IIa因子的活性,以及与依诺肝素相近的分子量(表1)。
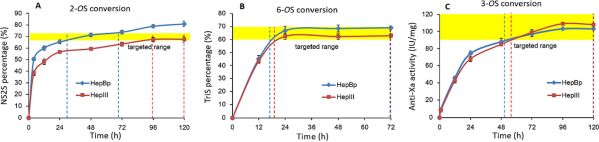
图3:酶促合成 LMWH 的磺基转移酶活性。A. NS2S通过2-OST酶和C5-epi反应转化;B.通过6-OST反应转化为TriS;C. 3-OST反应的抗Xa活性。
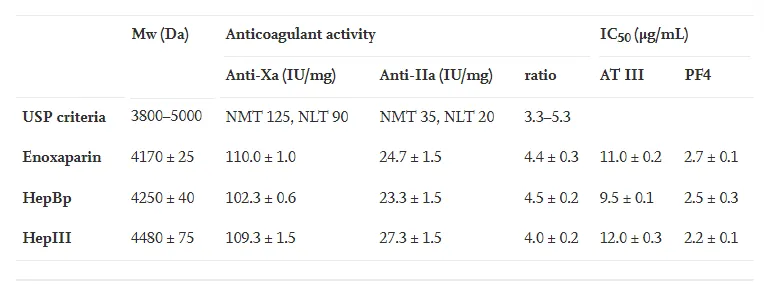
表1:LMWH 的抗凝活性和 IC50 值
为了进一步验证酶促合成的LMWH产物与依诺肝素的相似性,作者对两种LMWH进行了二糖组成和NMR分析。结果表明,被HepBp或HepIII降解并通过酶促修饰获得的LMWH,其二糖组成与依诺肝素相似。HepBp或HepIII降解的LMWH的NS2S6S含量的二糖分别为71.2±0.91%和60.1±0.60%(表2)。核磁共振分析也表明,两种不同的酶切生物催化LMWH具有相似的结构(图4B)。其中,5.8 ppm的氢信号为ΔU2S的H4,这代表非还原端存在不饱和糖醛酸残基,这也在核磁水平上证明了HepBp处理得到的LMWH不存在非还原端不饱和的糖醛酸。
表2: 二糖和四糖成分分析


图4:A. HepBp裂解的LMW-NSH的1H NMR;B. LMWH (HepBP)、LMWH (HepIII) 和依诺肝素的1H NMR。
最后,作者通过表面等离子共振 (SPR) 分析,检测了所获得的的LMWH与AT(抗凝血酶III)和PF4(血小板因子Ⅳ)的结合能力,以进一步评估LMWH的抗凝血能力。结果显示,酶促合成的LMWH与AT和PF4的结合亲和力与依诺肝素相似(图5),并且,HepBp切割得到的饱和非还原末端 LMWH 似乎不影响其与PF4结合。
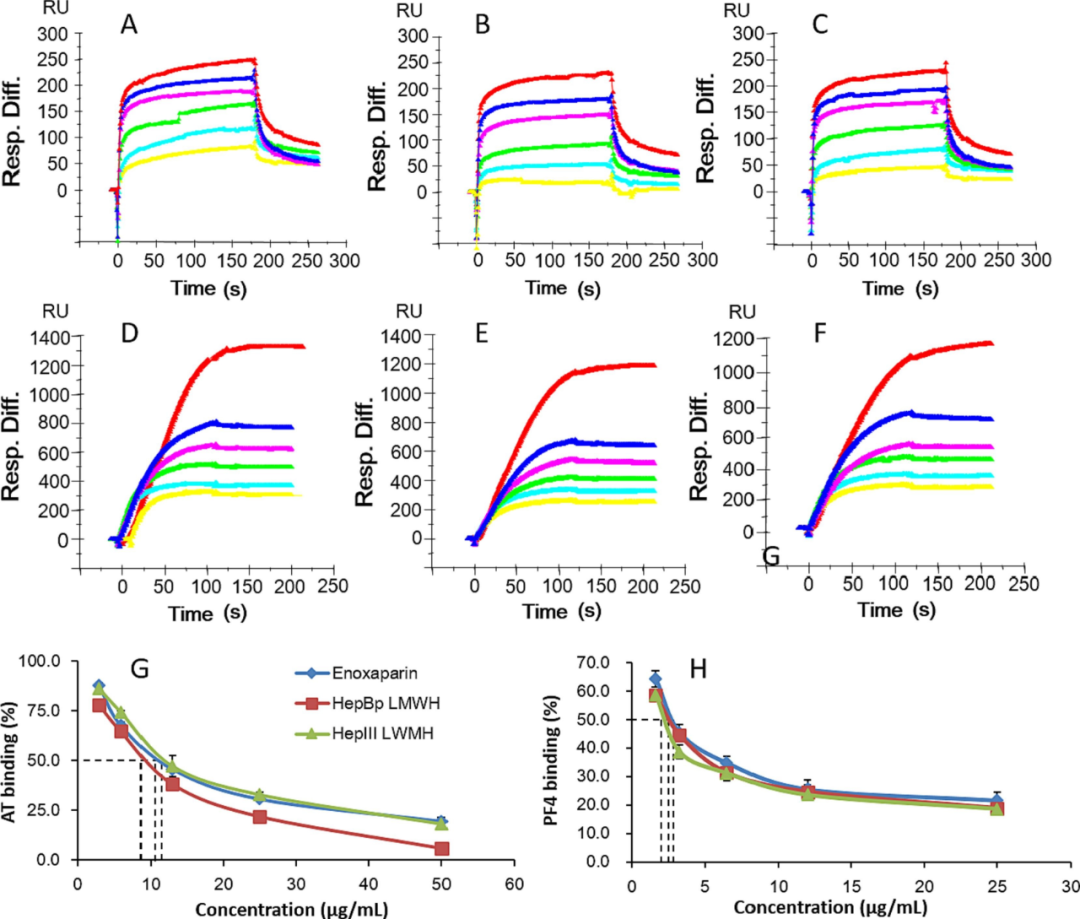
图5:不同LMWH样品的竞争性SPR分析。A. 依诺肝素和 AT;B. HepBp-LMWH 和 AT;C. HepIII-LMWH 和 AT;D. 依诺肝素和 PF4;E. HepBp-LMWH 和 PF4;F. HepIII-LMWH 和 PF4;G. AT 结合的 IC50;H. PF4 结合的 IC50。
原文链接:
https://www.sciencedirect.com/science/article/abs/pii/S0144861722007305
作者:汪浩
审核:李全才,吕友晶
编辑:邵萌
如有侵权,请联系删除