邮箱地址
前沿资讯
发布时间:2024-03-04 10:09:59 作者:青岛海大海洋寡糖科技有限公司 来源:本站
文章题目:Chemoenzymatic synthesis of sulfur-linked sugar polymers as heparanase inhibitors
发表期刊 : Nature Communications
影响因子 : 17.694(2021)
通讯单位 : 伦斯勒理工学院; 俄克拉荷马大学

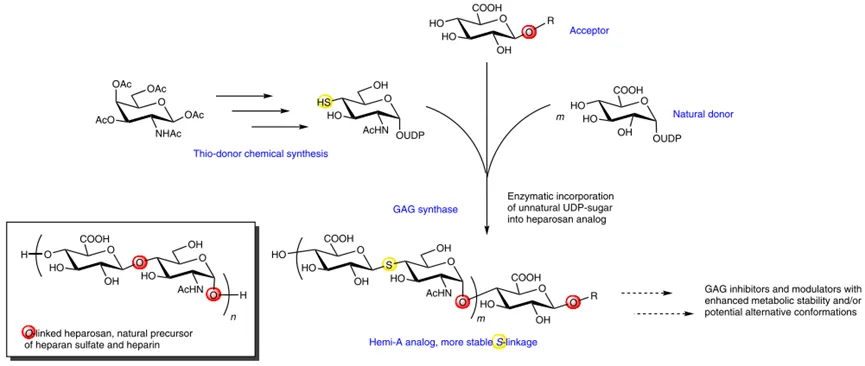
硫代糖苷,由于具有相比于天然糖苷低得多的酸催化和酶促降解速率,使其成为糖苷酶抑制剂的良好候选化合物。例如,异丙基硫代半乳糖苷(IPTG)是不可水解的乳糖操纵子转录诱导剂,已经广泛应用于重组蛋白的表达。S糖苷键和O糖苷键的长度和角度不同,能够在糖单元之间提供高度的灵活性,使硫代糖苷化合物在与蛋白质相互作用时,可以很容易地改变其构象,使其更好地适应催化部位。目前,已经开发了各种化学和酶学方法来合成简单的硫代糖苷。其中,C6位硫酸化的硫酸肝素的二糖类似物GlcA-S-GlcNAc,表现出较优越的肝素酶抑制活性。在这篇文章中,作者通过化学法成功合成了UDP-4-SH-GlcNAc,并将其作为糖基供体用于制备非还原性末端具有4-SH-GlcNAc的肝素类似物,除此之外,这些具有4-SH-GlcNAc末端的肝素类似物可继续作为酶促反应的糖基受体,用于构建含有非天然硫代糖苷键的肝素类似物。
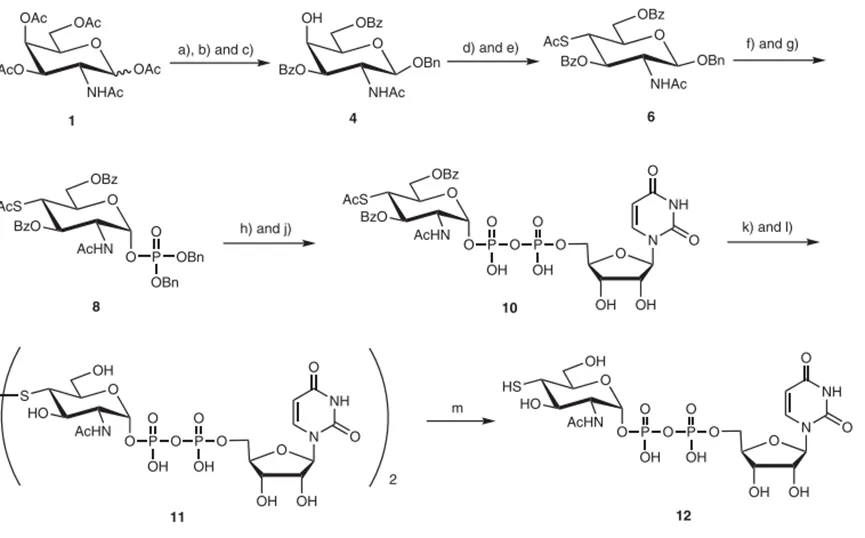
Figure 1. Chemical synthesis of the unnatural donor, UDP-4-SH-GlcNAc 12.
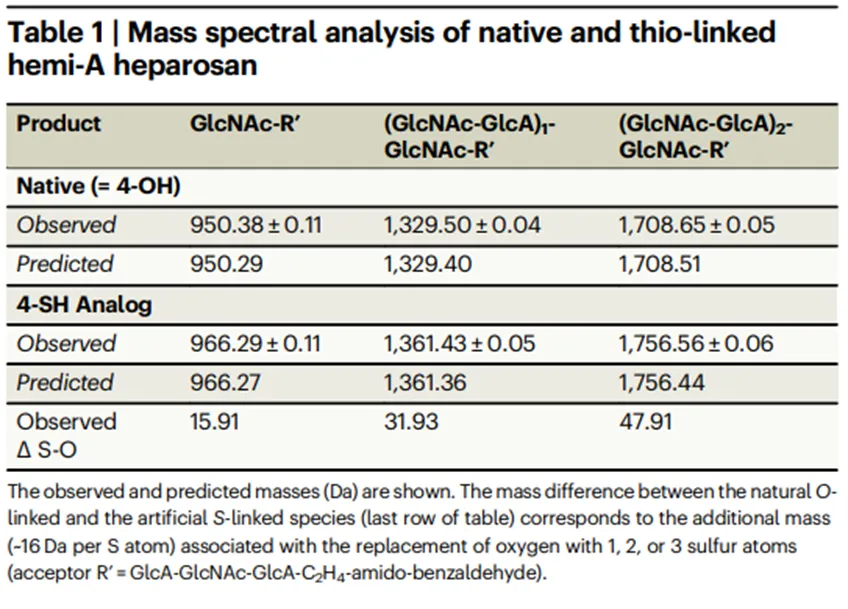
全乙酰GlcNAc经过正交脱保护以及C4位的构型翻转,获得了全保护的中间体8,用氢气脱出Bn,然后经过三步反应得到受保护的中间体10。继续进行保护脱除后,用氧气处理,得到二硫化的衍生物11,它比UDP-4-SH-GlcNAc 12更稳定,更容易纯化。将衍生物11使用还原剂二硫苏糖醇(DTT)打开二硫键,从而得到相应的供体UDP-4-SH-GlcNAc 12。获得可用于酶促糖基化的UDP-4-SH-GlcNAc 12后,作者通过MALDI-TOF质谱分析糖基转移酶能否有效识别12,从而构建S糖苷键连接的肝素衍生物。结果显示,中间体12可被有效转移至受体的非还原末端,获得具有4-SH-GlcNAc的寡糖产物;进一步研究发现,具有4-SH-GlcNAc末端的肝素类似物可继续作为酶促反应的糖基受体,从而构建含有GlcA-S-GlcNAc重复单元的肝素类似物(Table 1)。
Table 1. Mass spectral analysis of native and thio-linker hemi-A heparosan.
硫酸化修饰,特别是C6的硫酸根基团对肝素酶的识别似乎非常重要,因此对酶促合成的含有S糖苷键的肝素类似物进行了不同形式的硫酸化修斯。含有6-O-sulfo和2-O-sulfo的4-硫代肝素类似物是在碱性水溶液中,使用三氧化硫·三甲基胺对底物进行化学硫酸化制备的;与此同时,含有6-O-sulfo和NS的4-硫代肝素类似物通过两种磺基转移酶NDST和6-OST介导的两步酶促过程制备的(Figure 2)。
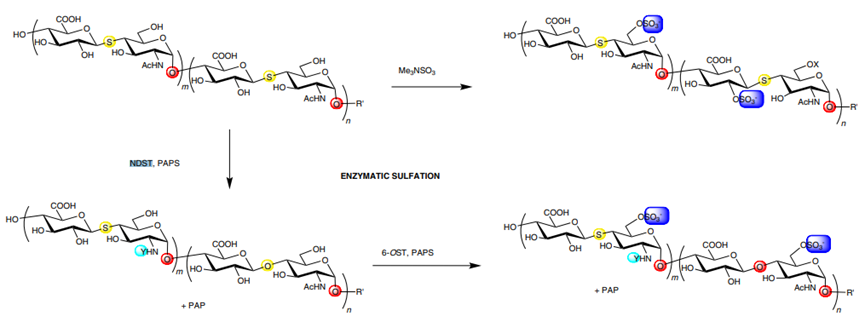
Figure 2. Synthesis of sulfo-4-thio-HS analogs.
接下来,作者进一步研究了制备的不同硫酸化4-硫代肝素类似物对人源肝素酶的抑制作用。研究发现,重组人肝素酶只降解硫酸化O-连接的肝素和天然HS,但不裂解硫酸化4-硫代肝素类似物(Figure 3b)。此外,硫酸化4-硫代肝素类似物能够有效抑制肝素酶对O-连接底物的消化(Figure 3c),并保护天然HS不被人类肝素酶消化,从而证明硫酸化4-硫代肝素类似物作为一种竞争性肝素酶抑制剂,具有潜在的肿瘤治疗价值。
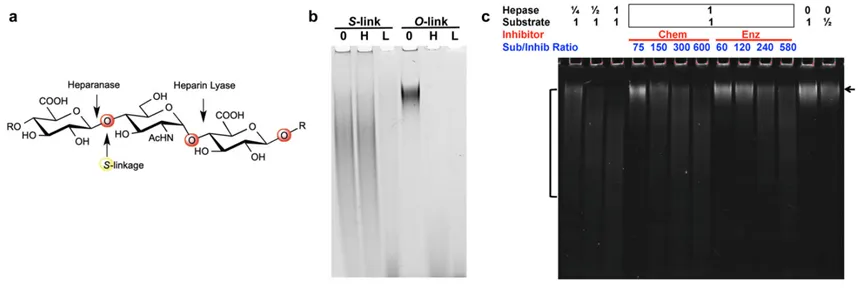
Figure 3. O-sulfo-S-linked heparosan analog enzyme challenges and inhibition.
总结:
本文介绍了一种化学酶法制备S-连接的肝素类似物的方法,通过该方法制备肝素类似物相比于相似结构的O-连接的肝素化合物,其肝素酶抑制活性提高了200-300倍。但是,UDP-4-SH-GlcNAc毕竟不是糖基转移酶的天然底物,反应效率较低,作者虽通过扩大反应体系、使用重组的嵌合合成酶、对多种反应条件进行优化,以提高产率,但产率仅略微提高。因此,未来可能需要构建更高效的工程化合成酶,以实现产业化的需求。
原文链接:https://www.nature.com/articles/s41467-022-34788-3
作者:汪浩
审核:李全才,吕友晶
编辑:邵萌
如有侵权,请联系删除